Когда клонируют найденного в Якутии мамонта?
Ученые уверены, что клонирование животных в скором времени поможет воскресить даже вымерших мамонтов, ведь для этого у них есть ДНК мамонта, останки которого с жидкой кровью нашли в 2013 году в Якутии. И хотя возраст вымершего мамонта составляет не менее 28 тысяч лет, тело погибшей самки частично находилось в озере, которое очень быстро замерзло и, таким образом, хорошо сохранилось. Этим научным экспериментом даже заинтересовался Владимир Путин, хотя якутские ученые пока никаких гарантий на возрождение мамонта не дают, однако планируют, как минимум, использовать его ДНК для сохранения слонов, которые вымирают.
Читайте далее: Собаки президента: история питомцев Путина и их политическое значение
Пока клонирование животных сложно поставить на поток, ведь не каждый любящий хозяин может выложить десятки тысяч долларов для создания клона домашнего любимца. Поэтому большинству людей остается просто смириться со смертью питомца и, может, завести себе нового друга.
КОТ ЗА 17500 ДОЛЛАРОВ
Китай приступил к клонированию животных еще в 2000 году и создал крупнейшую в мире фабрику копирования животных. Поначалу там рассчитывали получать в год миллион клонированных элитных коров и скакунов. Но вскоре там пришли к мысли, что можно неплохо заработать на копировании домашних питомцев – всем известно о привязанности к ним хозяев. И компания Sinogene стала предлагать «вернуть к жизни» отошедшего в мир иной питомца.
Первого кота клонировали за 35 000 долларов в 2019 году. Сейчас стоимость услуг снизилась. Клонирование кошки стоит 17 500 долларов, собаки – около 29 000. Возникла большая конкуренция среди компаний по клонированию, и они вынуждены снижать цены. По данным на 2021 год, в Китае содержат более 112 миллионов домашних питомцев, их число особенно увеличилось во время пандемии, и всех их владельцев убеждают быть готовыми купить клон любимой зверюшки.
История клонирования
Первый успешный проект клонирования млекопитающего – овечки Долли – датирован 05.07.1996 г. Его реализовали в Шотландии. Но первые клоны-зародыши были получены в 1892 году, когда Ганс Дрейш сумел разделить двуклеточный эмбрион морского ежа на две отдельные клетки, и повторил опыт с четырехклеточным. Все ежи выросли. Но Долли первое млекопитающее, выращенное из ДНК взрослой особи, а не эмбриона. Еще одно отличие овечки, она первое животное, созданное при вмешательстве в ядерную структуру клетки.
Прорыв Яна Вильмута «создателя» Долли в том, что он проводил эксперименты не с зародышами или молодыми особями, а воспользовался генетическим материалом взрослой 6-летней овцы. Он взял клетки с неизмененной нативной структурой ДНК из молочной железы. Подождал прекращения деления и извлек из них ядро. Затем поместил их в яйцеклетку другой особи. Для опыта использовали 277 оплодотворенных клеток, выжила только одна. За вклад в науку Вильмут получил рыцарское звание, присвоенное королевой Елизаветой II.
На сегодня генной инженерией клонированы:
| Год | Животное |
| 1970 | Лягушка |
| 1985 | Рыба |
| 1986 | Мышь из клеточного материала эмбриона |
| 1996 | Овца из клеточного материала взрослой особи |
| 1998 | Корова |
| 1999 | Коза |
| 2000 | Обезьяна, свинья с органами пригодными к трансплантации человеку |
| 2001 | Кошка, с 2005 начато воспроизводство в коммерческих целях |
| 2002 | Кролик |
| 2003 | Олень, бык, мул |
| 2004 | Собака, с 2008 начато воспроизводство в коммерческих целях |
| 2004 | Бантенг, исчезнувший вид азиатских диких быков |
| 2006 | Хорек |
| 2009 | Верблюд |
| 2009 | Букардо, исчезнувший вид горного пиренейского козла |
| 2011 | Койот |
| 2018 | Макаки |

В 1999 году главная тема ученого бомонда – самочувствие овечки Долли. Изучение ее организма давало неутешительные прогнозы: организм с самого рождения, по неподтвержденным данным, был излишне состарен. Идея использовать клонированные объекты для лечения наследственных заболеваний или рака отходит на задний план.
С 2000 года значение понятия «клон» трансформируется в генетического близнеца, отсроченного по времени. В Японии проведен эксперимент появления клона животного из генов, ранее созданного клона. В Канаде с 2000 ведутся работы по выращиванию клонированного человеческого органа.
14.02.2003 года мир узнал об умерщвлении овечки Долли, причина прогрессирующее заболевание легких. Ученые разделились на 3 лагеря в установлении причин болезни клонированного животного:
- Часто овцы, живущие в неволе, страдают подобными заболеваниями.
- Неспособность теломеров, концевых участков хромосом, соединяться.
- Клонирование стало причиной ускоренного старения.
Чучело овцы было выставлено в музее Шотландии.

Пять тысяч подопытных собак за один удачный клон
Опыты с Долли и Мисси показали, что клонировать млекопитающего можно с использованием клеток уже взрослых животных. Проблемой оказалось количество неудачных попыток: зародыши Snuppy подсаживали 123 суррогатным матерям, прежде чем родилась здоровая собака, а недостаток подопытных псов Хоутрон называл одной из причин провала работы в США. При этом часть собак погибли во время имплантации эмбриона или вскоре после неё, поскольку получали сильную гормональную терапию, приводившую к отказу внутренних органов.
Бизнесмен оценивал количество собак у техасцев на уровне 80 особей одновременно, а у корейцев приблизительно в 5000 подопытных. Американцы самостоятельно так и не приблизились к рождению живой собаки, постоянно сталкиваясь с мертворождёнными щенками или гибелью суррогатных матерей. Опыты с другими млекопитающими давали схожий результат.
Свинья по кличке Xena выведена в 2001 году по «технике Гонолулу». Учёным понадобилось подселить 110 эмбрионов двум суррогатным матерям, прежде чем появился живой клон Фото Денниса Нормайла
В 2003 году учёные техасской компании Viagen начали изучать вымирающие виды с целью клонирования, а в 2016 году подразделение Pets предложило всем желающим клонировать собаку за 50 тысяч долларов или кота за 25 тысяч долларов. Клонирование кошек дешевле, поскольку у них менее сложная репродуктивная система и выше вероятность получить кошку с другим окрасом и характером, что скажется на её внешнем виде.
Хозяин приобретает специальный набор для взятия генетического материала животного и отправляет образцы в Viagen, где клетки замораживают в жидком азоте. Когда клиент решит, что пришло время, компания начинает процесс клонирования по алгоритму выведения Долли. Иногда получаются две одинаковые особи, тогда оба клона передаются хозяину.

В 2018 году Барбара Стрейзенд клонировала умершую собаку Саманту, получив два очень похожих на оригинал клона (на фото по краям, в центре сестра оригинальной собаки). Позже певица призналась, что у клонов совершенно другой характер Фото из профиля актрисы в Инстаграм
22-летний китаец Хван Ю похоронил своего кота по кличке Чеснок, а через несколько часов прочитал статью о клонировании животных. Позже он выкопал похороненного, упаковал и положил в холодильник, ожидая представителя компании, которая клонирует его питомца. На свет появился очень похожий на Чеснока клон, но у него нет примечательного чёрного пятна на подбородке. Мужчина не скрывал разочарования, но сказал, что понимает ограничения технологии.
Владельцы клонированных животных часто испытывают смешанные чувства по поводу новых питомцев: иногда клоны визуально отличаются незначительно, но характер животного обычно совсем другой. Собаки могут лаять и скулить как оригинальный пёс, но обладают другим темпераментом.
Биоэтики и ветеринары напоминают желающим клонировать любимца о последствиях: для достижения цели могут погибнуть несколько суррогатных матерей, а приюты по всему миру по-прежнему переполнены бездомными животными.
Сомнительные результаты клонирования домашних питомцев подталкивают бизнесменов искать новые пути заработка, где количество заказов не зависит от эмоций клиентов. Клонированные лошади для игры в поло не раз помогали выигрывать спортивные состязания, и теперь клиенты заинтересованы в копировании самых эффективных особей своего вида. При этом опытные наездники скептически относятся к клонам, указывая генетику только как один из факторов успеха.
Помимо спортсменов, постоянными заказчиками клонов становятся силовики. Клонированные собаки служат в Китае и Южной Корее. Желая сохранить природные способности животных и сократить время обучения, полиция и вооружённые силы уже несколько лет участвуют в программе клонирования.
Офицеры рассказывают, что щенки очень похожи на прародителей как внешне, так и по повадкам. Опробованные на оригинальных собаках программы дрессуры позволяют усовершенствовать упражнения и существенно быстрее обучать псов новым навыкам.

Офицеры полиции вместе с шестью клонированными щенками Фото Пекинского муниципального бюро общественной безопасности
Sooam Biotech Research Foundation сотрудничали с Российским военно-историческим сообществом и полицией. Корейцы передали двух кобелей-клонов бельгийского малинуа на службу в МВД Якутии, но собаки не адаптировались к морозу и провалили тренировочные задания.
Почему фермеры снова забили тревогу (хотя это не связано с ГМО)?

Еще в 2006 году Управление по контролю за едой и лекарствами США начало проверку клонированного скота. Американцы обеспокоились безопасностью мяса дублированных животных. Волновались не только потребители, но и фермеры, которые понимали явные преимущества крупных производителей. Появись у компании корова, зарекомендовавшая себя как прекрасный образец вкуснейшей мраморной говядины, владелец тут же бы начал ее клонировать, поставляя на рынок «безупречный вкус» или любой другой красивый рекламный слоган.
О своем намерении клонировать крупные партии животных заявило несколько американских компаний и одна китайская под названием The Boyalife Group. В 2016 году ее представители объявили о том, что в ближайшее время они планируют выпускать сто тысяч клонированных коров ежегодно, а к 2020 году увеличить их число до миллиона. О своих успехах китайские производители с тех пор не сообщали, но, учитывая последний удачный опыт, вероятно, что среди вывозимой из Поднебесной говядины были и кусочки клонов.
Реклама ViaGen. Заменить коров на людей — и будет настоящий киберпанк
В Соединенных Штатах тоже работает сразу несколько успешных фирм, среди которых техасская ViaGen завоевала наибольшую известность. В 2008 году Управление по контролю за едой и лекарствами проверило их мясо и пришло к выводу, что опасаться нечего, хотя скептиков осталось предостаточно. Сегодня ViaGen — едва ли не крупнейшая компания, занимающаяся выращиванием клонированных животных больше 15 лет.
Удачные примеры домашних питомцев, рождённых «из пробирки»
Ни одна клиника не называет точных цифр и не выдаёт тайну о том, сколько животных они клонируют ежегодно. Эта информация является строго конфиденциальной. Если следить за новостями, происходящими в мире, можно сказать, что этот показатель достаточно высок. Так, регулярно появляется информация о вновь клонированном домашнем питомце. Естественно, это дорогостоящий процесс, и доступен он только обеспеченным заводчикам.
Вечные домашние питомцы
17 октября 2004-го года американской клиникой Genetic Savings and Clone был клонирован 17-летний мейн-кун Ники. Его хозяйка Джулия потратила 50 000$ на то, чтобы воссоздать точную копию своего преданного любимца, который умер за год до появления клона. Как говорит сама заводчица, клон полностью унаследовал характер предшественника.
Мейн-кун Ники — кот, клонированный в США по заказу хозяйки Джулии
В 2008–2009-м годах в Южной Корее был клонирован лабрадор Чейс, которого таможенники считали лучшей ищейкой. На эти цели из бюджета страны было выделено 240 000$. В результате процедуры на свет появилось 7 щенков.

Всем семерым клонам была дана кличка Топпи
В 2014-м году компания Sooam Biotech в Южной Корее организовала конкурс среди владельцев кошек и собак. Основное условие конкурса — отправить видеоролик с участием питомца, приз — возможность клонировать своего любимца. Победу одержали американка Ребекка Борн и её такса по кличке Винни. В результате на свет появилась маленькая копия таксы — Минни-Винни. Роды проходили путём кесарева сечения. Хозяйка говорит, что Минни-Винни ничем не отличается от «оригинала», так как полностью сохранила характер и повадки Винни. В 2018 году Мини-Винни родила двух щенят.

Клон Винни появился на свет после кесарева сечения, и Ребекка сказала, что малышка выглядела точно так же, как и «мама-оригинал»
В 2017 году голливудская звезда Барбра Стрейзанд клонировала свою любимицу породы котон-де-тулеар, которая умерла в возрасте 14 лет. В результате процедуры на свет появились два щенка — мисс Вайолет и мисс Скарлетт. Как заметила сама звезда, характеры питомцев сильно отличаются от характера их предшественницы.
В доме у Барбры Стрейзанд живут два клона её предыдущей любимицы и один щенок, появившийся на свет естественным путём
Многие обеспеченные люди стараются продлить жизнь своему питомцу, поэтому прибегают к клонированию. Но я считаю, что это крайне эгоистично, ведь в этот момент они думают только о своих чувствах. Ведь ни о каком продолжении жизни в этом случае речи не идёт. Они всего лишь получают приближённую копию своего любимца, который может иметь совершенно иные нрав и характер по сравнению с «оригиналом». На сегодняшний день на улицах городов бегает большое количество брошенных питомцев, которые нуждаются в помощи и ласке. Поэтому деньги, потраченные на клонирование, можно было бы потратить с большей пользой и тем самым помочь «бродяжкам».
Видео: боксёры-близнецы как результат успешного клонирования
На сегодняшний день клонирование — процедура, доступная только обеспеченным заводчикам животных. Получение положительного результата возможно исключительно в условиях лаборатории, поэтому проведение домашних экспериментов нецелесообразно, особенно если человек не обладает специальными умениями и навыками.
Понятие и сущность клонирования
Одним из ярких примеров достижений ученых, с проблемой которого человечеству придется столкнуться не раз, является клонирование.
Клонирование – это процесс, в котором живое существо производится из одной клетки, взятой у другого живого существа.
Клонирование обычно определяется как производство клеток или организмов с теми же ядерными геномами, что и у другой клетки или организма. Соответственно, путем клонирования можно создать любой живой организм или его часть, идентичные уже существующим или существующим, если сохранилась информация о его ядерных геномах.
Еще несколько десятилетий назад клонирование было больше предметом дискуссий для писателей-фантастов, чем научные дискуссии или социально-политические дебаты. Бурное развитие генной инженерии и как раз расцвет биотехнологии в 1990-е годы создали все условия для практической возможности клонирования живых существ. Научно-технический прогресс, как это часто бывает, сделал все реальностью.
Клонирование взрослых млекопитающих.
По мере роста и развития животного соответствующие его гены «включаются» и «выключаются» в строго определенное время, что обеспечивает гармоничное формирование и функционирование всех частей сложного организма. У взрослой особи гены, регулирующие процессы в специализированных (дифференцированных) клетках, должны работать без сбоев, выполняя характерную именно для этой части тела программу: малейшее нарушение здесь чревато болезнью, а то и гибелью всей особи. Следовательно, если вырезать кусочек, скажем, уже сформировавшегося подбородка, нос из него не разовьется. Правда, клетки могут терять специализацию (дедифференцироваться), что наблюдается при возникновении раковых опухолей. Таким образом, клонирование животных из их взрослых клеток путем перепрограммирования последних на нормальное эмбриональное развитие представляет собой хотя и выполнимую теоретически, но крайне сложную задачу, которую многие специалисты считали неразрешимой.
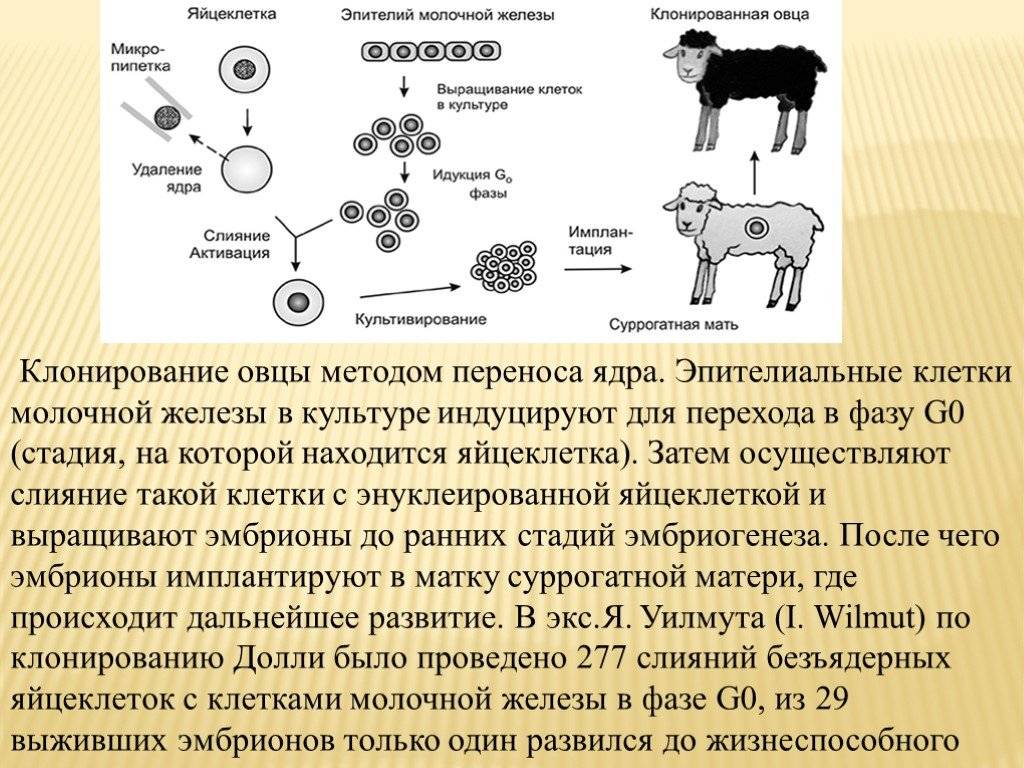
В 1997 шотландский эмбриолог Ян Уилмат со своими сотрудниками сообщил об успешном клонировании ягненка из дифференцированной клетки молочной железы шестилетней овцы. Культивируя клетки этого типа на т.н. минимальной (содержащей лишь минимум необходимых для поддержания жизни веществ) питательной среде, не позволявшей им выполнять свои «взрослые» функции, удалось добиться их дедифференцировки до эмбрионального состояния. Затем такую клетку слили с энуклеированной (лишенной ядра) яйцеклеткой другой овцы и имплантировали начавший развитие эмбрион в матку третьей самки. В результате исходная клетка молочной железы повторила и самостоятельно отрегулировала все этапы, которые в норме проходит оплодотворенное яйцо, превращаясь во многие миллиарды специализированных клеток взрослого млекопитающего. Через некоторое время эти исследователи сообщили о клонировании овцы с введенным в нее человеческим геном, а специалисты из США заявили о создании клонов взрослых коров.
Важно подчеркнуть, что особи получаемых описанным способом клонов не достигают того уровня идентичности друг другу, который свойствен однояйцовым близнецам. Во-первых, развитие их происходит в разных ооцитах, каждый из которых сохраняет некоторое количество собственной ДНК в митохондриях (органеллах дыхания). Во-вторых, эмбрионы вынашиваются различными «приемными матерями», и, наконец, после рождения каждый детеныш попадает в условия среды, неизбежно являющиеся в той или иной степени уникальными
Во-вторых, эмбрионы вынашиваются различными «приемными матерями», и, наконец, после рождения каждый детеныш попадает в условия среды, неизбежно являющиеся в той или иной степени уникальными
Во-вторых, эмбрионы вынашиваются различными «приемными матерями», и, наконец, после рождения каждый детеныш попадает в условия среды, неизбежно являющиеся в той или иной степени уникальными.
Клоны среди нас
Однако и такой подход, говоря словами первооткрывателя структуры ДНК Джеймса Уотсона, представляет собой позицию человека, который, стоя по горло в воде, открывает над собой зонтик. Ни один искусственно клонированный человек не родился на свет, но среди нас жили и живут десятки миллионов самых настоящих клонов. Имя им — однояйцевые близнецы.
Выше уже говорилось, что если после первого деления зиготы получившиеся клеточки разъединить, то из каждой вырастет полноценный эмбрион, а затем и организм. Иногда (у человека примерно в одном случае из трехсот) этот процесс происходит самопроизвольно. И тогда на свет появляются два (а порой и больше) генетически идентичных организма с одинаковыми отпечатками пальцев, абсолютной иммунной совместимостью и чрезвычайно сходной внешностью. Каждый из них является клоном другого, и если догмат о воссоединении души с телом в момент оплодотворения понимать буквально, то у них должна быть одна душа на двоих.
Вопрос о душе, конечно, схоластический, но нетрудно видеть, что этические проблемы клонирования уже решены однояйцевыми близнецами. И прежде всего — проблема уникальности человеческой личности, угрозу которой почему-то увидели в клонировании. Сколь бы ни были похожи друг на друга близнецы, как внешне, так и по своим вкусам, пристрастиям, темпераменту, все прекрасно понимают, что это не два экземпляра одного человека, а две отдельные личности. У каждого из них свой собственный жизненный путь, единственный и неповторимый.
Справедливости ради следует сказать, что заслуживающие внимания возражения против клонирования человека все-таки есть. Как уже говорилось, те клонированные организмы, которым удалось появиться на свет, чаще болеют и менее жизнеспособны, чем их обычные сородичи. Клонирование человека сегодня означало бы намеренное рождение больных детей. И это была бы ничем не оправданная жестокость, ибо за все эти годы никто так и не смог назвать разумной цели, для достижения которой нужны люди-клоны. Исходя из этих соображений, запреты на клонирование человека можно было бы признать разумной мерой, если бы они касались лишь создания целого человеческого организма. К сожалению, многие из запретов не делают разницы между репродуктивным и терапевтическим клонированием. Последний термин означает получение популяции эмбриональных клеток, генетически идентичных клеткам определенного человека.
Вообще говоря, культуры человеческих клеток успешно создавались и создаются без манипуляций с ядрами. Однако пересадив ядро зрелой клетки в яйцеклетку и позволив ей несколько дней развиваться в пробирке, можно получить бластоцисту — шарик из нескольких сотен клеток, значительную часть которых составляют эмбриональные стволовые клетки. Если бы бластоцисте позволили прикрепиться к стенке матки, из этих клеток развились бы все ткани и органы будущего организма. Но можно ли вне организма выращивать изолированные органы и заменять ими по мере надобности больные органы «оригинала»? Это сняло бы сразу две тяжелейшие проблемы современной трансплантологии: иммунной совместимости (поскольку все клетки выращенных «в пробирке» органов будут нести гены их будущего получателя) и нехватки доноров.
Десять лет назад все это выглядело чистой фантазией, хотя о принципиальной возможности такого «самодонорства» ученые говорили уже тогда. Сегодня медицина значительно продвинулась в этом направлении: из стволовых клеток удается получать не только отдельные ткани, но и сложные многотканевые структуры, такие как участки сосудов или купол мочевого пузыря. Однако для того, чтобы создать столь сложный орган, как сердце, нужны именно эмбриональные стволовые клетки, способные к превращению в любую ткань организма. И хотя уже несколько лабораторий объявили о получении таких клеток без пересадки ядер, пока что самым обнадеживающим источником их остается терапевтическое клонирование.
Перспективы, которые оно открывает, столь заманчивы, что развитые страны одна за другой включаются в эту гонку, несмотря на протесты религиозных кругов и принятую ООН в 2005 году декларацию, осуждающую всякое клонирование. Терапевтическое клонирование официально разрешено в Великобритании (где ряд лабораторий уже оформил соответствующие лицензии), Бельгии и Швеции , в конце прошлого года к этому списку присоединилась и Австралия. Весьма вероятно, что после выборов 2008 года (кто бы их ни выиграл) запрет на терапевтическое клонирование будет снят и в США.
Десять лет назад клонирование воспринималось как сенсация, чудо или жупел. Сегодня оно все больше становится одной из доступных человечеству технологий.
Терапия будущего
Быть лучшим человеком
Этический аспект клонирования животных поднимается каждый раз, когда учёные объявляют о новых достижениях. Биоэтика рассматривает в первую очередь страдания суррогатных матерей и потенциал исследований клонирования млекопитающих для клонирования человека. Несмотря на то, что сейчас требуется значительно меньше подсадок яйцеклеток с заменённым ядром, истинные масштабы мертворождения клонов и смерти матерей неизвестны.

Протесты в 2002 году около офиса калифорнийской компании Geron Corportaion, которая работает над лекарствами для лечения онкологии из стволовых клеток, получаемых из человеческих эмбрионов Фото Getty
В 2005 году ООН приняла резолюцию, запрещающую клонирование человеческой особи. В некоторых странах, включая Россию, эксперименты с клонированием человеческих клеток запрещены полностью и бессрочно. Тем не менее, учёные регулярно работают с эмбриональными стволовыми клетками, которые получают из оставшихся от ЭКО-процедур эмбрионов. При этом зародыш даже теоретически не может что-то ощущать — забор производится у пятидневного эмбриона, который представляет собой шар из клеток (бластоцисту).
Фактически в мире действует запрет на перенос ядер человеческих соматических клеток, но основной проблемой в клонировании человека считается даже не юридический аспект. Только в 2018 году в Китае клонировали яванских макак, геном которых максимально похож на человеческий. ДНК приматов существенно отличается в деталях, поэтому «метод овечки Долли» сработал только после точечного программирования клеток.
Учёные отмечают, что эксперименты с женщинами, которым будут подсаживать эмбрионы в таких количествах, просто немыслимы. Теоретически сначала должны создать идеального клона, который с большой вероятностью приживётся, но это невозможно без экспериментов. Поэтому пока в клонировании человека и его клеток наука развивается в так называемом терапевтическом клонировании. Учёные научились получать стволовые клетки из крови и кожи взрослых, перепрограммировать их и воссоздавать из них молодые стволовые клетки.
В перспективе такие исследования человеческих клеток могут привести к созданию лекарств от некоторых видов онкологии, болезни Альцгеймера и других серьёзных недугов. Но пока учёные пытаются убедить обывателей в отсутствии планов клонирования человека и безопасности копирования животных. Впрочем, часть из них уже давно переступила этическую черту заработка на питомцах, а богачи иногда задумываются о клоне человека.
Первые опыты на амфибиях
Возможность клонирования эмбрионов позвоночных впервые была показана в начале 50-х годов в опытах на амфибиях.
Большой вклад в эту область внес английский биолог Гердон. Он первым в опытах с южноафриканскими жабами Xenopus laevis (1962) в качестве донора ядер использовал не зародышевые клетки, а уже вполне специализировавшиеся клетки эпителия кишечника плавающего головастика. Ядра яйцеклеток реципиентов он не удалял хирургическим путем, а разрушал ультрафиолетовыми лучами. В большинстве случаев реконструированные яйцеклетки не развивались, но примерно десятая часть их них образовывала эмбрионы. 6,5% из этих эмбрионов достигали стадии бластулы, 2,5% — стадии головастика и только 1% развился в половозрелых особей.
Однако появление нескольких взрослых особей в таких условиях могло быть связано с тем, что среди клеток эпителия кишечника развивающегося головастика довольно длительное время присутствуют первичные половые клетки, ядра которых могли быть использованы для пересадки. В последующих работах как сам автор, так и многие другие исследователи не смогли подтвердить данные этих первых опытов.
Позже Гердон модифицировал эксперимент. Поскольку большинство реконструированных яйцеклеток (с ядром клетки кишечного эпителия) погибают до завершения стадии гаструлы, он попробовал извлечь из них ядра на стадии бластулы и снова пересадить их в новые энуклеированные яйцеклетки (такая процедура называется «серийной пересадкой» в отличие от «первичной пересадки»). Число зародышей с нормальным развитием после этого увеличивалось, и они развивались до более поздних стадий по сравнению с зародышами, полученными в результате первичной пересадки ядер.
Затем Гердон вместе с Ласки (1970) стали культивировать in vitro (вне организма в питательной среде) клетки почки, легкого и кожи взрослых животных и использовать уже эти клетки в качестве доноров ядер. Примерно 25% первично реконструированных яйцеклеток развивались до стадии бластулы. При серийных пересадках они развивались до стадии плавающего головастика. Таким образом было показано, что клетки трех разных тканей взрослого позвоночного (X. laevis) содержат ядра, которые могут обеспечить развитие по крайней мере до стадии головастика.
В свою очередь ДиБерардино и Хофнер использовали для трансплантации ядра недслящихся и полносгью дифференцированных клеток крови — эритроцитов лягушки.
После серийной пересадки таких ядер 10% реконструированных яйцеклеток достигали стадии плавающего головастика. Однако даже с помощью многократных серийных пересадок (более 100 клеточных циклов) реконструированные яйцеклетки дальше стадии головастика не развивались.
Таким образом, во многих работах показано, что в случае амфибий донорами ядер могут быть лишь зародыши на ранних стадиях развития. Некоторые авторы называют подобные эксперименты клонированием амфибий, хотя правильнее называть их клонированием эмбрионов амфибий, так как в этом случае мы размножаем бесполым путем не взрослых животных, а зародышей.
Дифференцировка клеток в ходе развития позвоночных сопровождается инактивацией неработающих генов. Поэтому клетки теряют тотипотентность, дифференцировка становится необратимой. В конце концов у одних клеток происходит полное репрессирование генома, у других — в той или иной степени деградирует ДНК, а в некоторых случаях разрушается даже ядро. Однако наряду с дифференцированными кочетками культивируемые in vitro клеточные популяции содержат малодифференцированные стволовые клетки, которые и могут быть использованы как доноры ядер для клонирования млекопитающих.
Опыты с амфибиями показали, что ядра различных типов клеток одного и того же организма генетически идентичны и в процессе клеточной дифференцировки постепенно теряют способность обеспечивать развитие реконструированных яйцеклеток, однако серийные пересадки ядер и культивирование клеток in vitro в какой-то степени увеличивает эту способность.
Немного истории клонирования
У клонирования сложный и тернистый путь.
Можно сказать, что одной из основ клонирования является клеточная теория, разработанная Теодором Шванном в 1839 году. В 1866 году вышла статья Грегора Менделя по селекции растений, в которой впервые говорится о «единице информации». Таким образом были заложены основы генетики. В 1886 году профессор-зоолог Московского университета А.А. Тихомиров обнаружил возможность развития шелковичного червя из неоплодотворенного яйца. В 1892 году Г. Дриш впервые изучил, что происходит с генетическим материалом клетки во время ее деления, на бластомерах морского ежа. Группой ученых также было доказано, что генетическая информация содержится в ядре. В 1902 году два независимых исследователя, У. Саттон и Т. Бовери, описали хромосомы и объявили, что «единицы информации» Менделя находятся в хромосомах. В 1909 году Вильгельм Йоханнсен дал название этим «единицам информации». С этого момента они стали называться генами. В том же 1909 году советский ученый-гистолог А.А. Максимов впервые использовал термин «стволовая клетка» для клетки, которая дает начало другим клеткам. В 1910 году Томас Хант Морган начал определять расположение различных генов в хромосомах мушек. Можно смело сказать, что указанные исследования внесли фундаментальный вклад в развитие всех наук о живом, а также заложили основы клонирования.
В 40-х годах прошлого века советский ученый-эмбриолог Г.В. Лопашов проводил эксперименты по переносу клеточных ядер в энуклеированную (лишенную ядра) яйцеклетку земноводных. Аналогичные работы с земноводными проводили эмбриологи Т. Кинг и Р. Бриггс в США. В 50-х годах английский эмбриолог Д. Гордон пересаживал ядра соматических клеток в яйцеклетки лягушки. В 1963 году Тонг Дизхоу получал клоны карпа. В 1975 году были опубликованы результаты успешной работы Д. Бромхола по клонирования кроликов. В 1983 году Л.А. Слепцова и ее коллеги клонировали костистых рыб (вьюнов). В 80-х годах прошлого столетия ученый С. Вилладсен провел серию успешных опытов по клонированию сельскохозяйственных животных путем переноса в яйцеклетку ядра зародыша. В 1997 году Йэн Уилмат и Кейт Кэмпбелл из Шотландии объявили о прорыве: проведено клонирование овцы с использованием соматической, не зародышевой, клетки , !
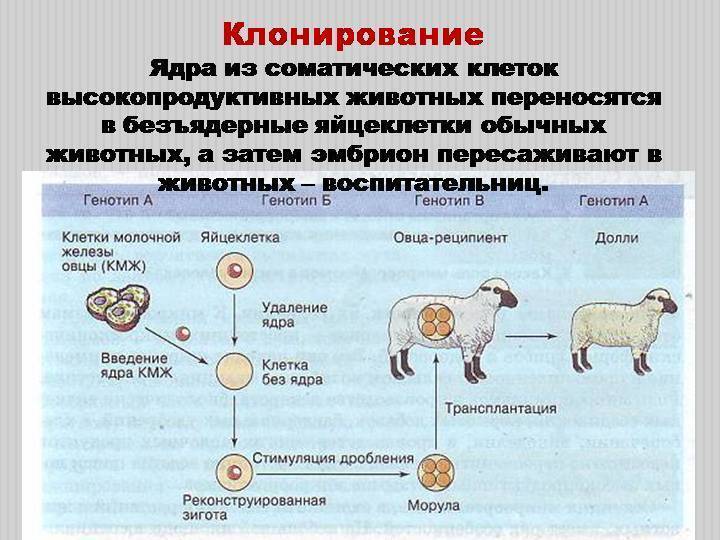
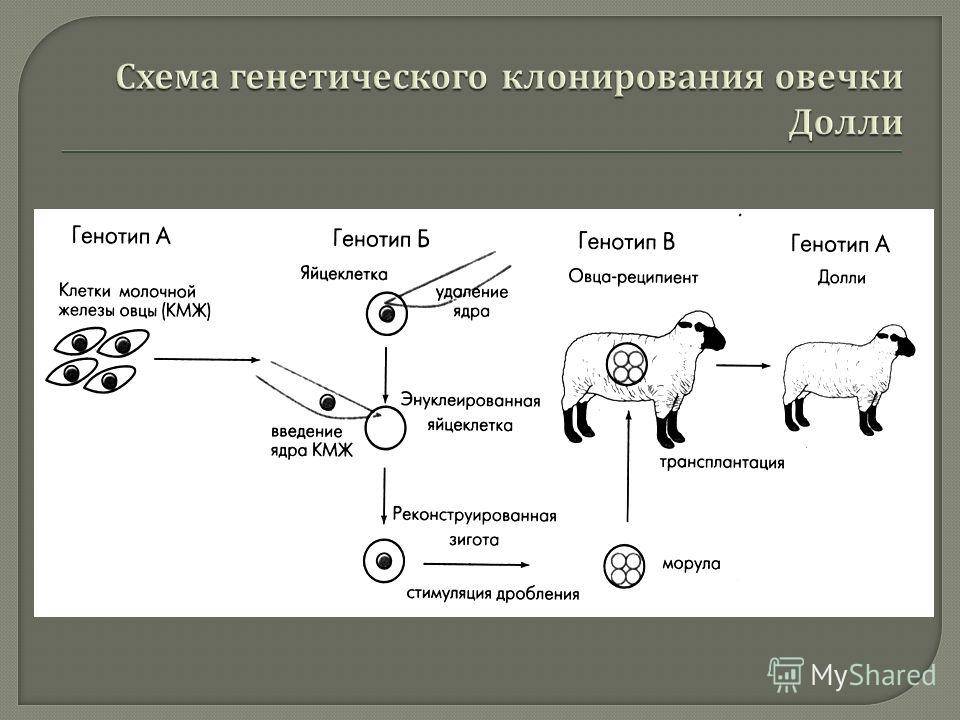
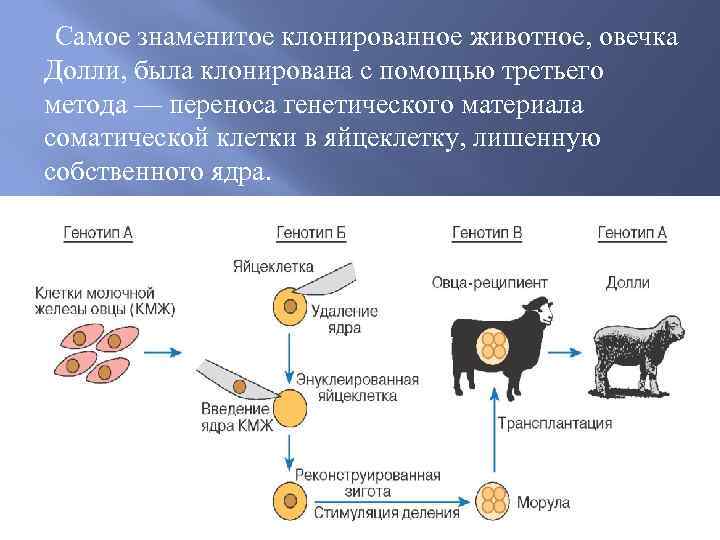
Долли — самка овцы, первое млекопитающее, которое смогли клонировать из зрелой соматической клетки путем замещения ядра. Технология получения этого клона была следующей.
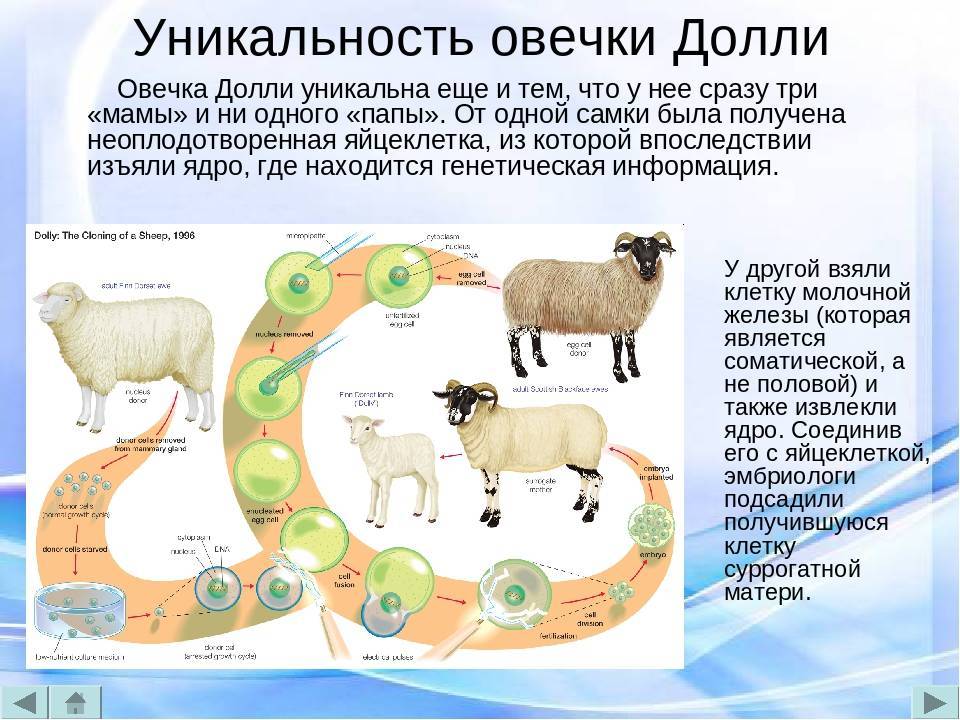
При клонировании Долли использовали клетки двух «родителей» и «суррогатную мать» — еще одну самку овцы. От одного «родителя» брали яйцеклетку, из которой удаляли ядро. От второго брали ядро, извлеченное из соматической клетки (вымени). Внутрь безъядерной яйцеклетки первой овцы вводили ядро зрелой соматической клетки другой овцы. Затем физическим (электрическим) методом провоцировали процесс деления и образования эмбриона (рис. 2). После чего эмбрион переносили в матку «суррогатной матери» — овцы.
Рисунок 2. Схема клонирования овцы Долли
Потребовалось очень много попыток клонирования, прежде чем на свет появилась Долли. Ученые — биологи из Шотландии Йэн Уилмат и Кейт Кемпбелл — по праву могут считать себя «Родителями» Долли . В 2003 году Долли пришлось усыпить из-за заболевания легких и артрита. После этого ее забальзамированное тело было выставлено в Королевском музее Шотландии.
В вопросе о клонировании остается много сложного и спорного. Необходимо соблюсти все этические нормы по отношению к живому . Но исследования наверняка будут продолжаться. А мы должны понимать, что за словом «клонирование» скрываются не научно-фантастические рассказы, а реальная технология, которая может принести и практическую пользу.
Например, клонирование может помочь получить животных и растения с необходимыми параметрами, такими как плодовитость, устойчивость к болезням. Опыты с клонированием могут помочь в лечении болезней. Очень интересной является перспектива использования клонирования для восстановления популяции вымерших или вымирающих видов. Отдельного внимания заслуживают опыты терапевтического клонирования — получение культуры стволовых клеток для разработки новых методов терапии тяжелых заболеваний, например, онкологических .